
发布日期: 2024-06-28 10:35:11 来源:新产品展示
2019年底,武汉市出现因新冠病毒感染导致的肺炎疫情,截至3月7日,全国累计已有超过8万人感染,并造成超过3000人死亡。
在疫情出现后,多家体外诊断公司声明研发出了用于新冠疫情诊断的试剂盒。在疫情爆发的初期,由于PCR检测试剂盒供应不足、检验能力不够等原因,导致湖北仍存在有疑似病例但难确诊的现象,有患者被告知暂时没有办法进行病毒检测,回家自行隔离。
随着慢慢的变多体外诊断公司开始供应核酸试剂盒,大量疑似病例得到确诊,但同时,关于新冠肺炎核算检验测试假阴性的问题开始引发讨论。
此外,核酸检验测试方法受制于试剂盒质量、能够承担临床检测的P3实验室(生物安全3级实验室)数量,P3实验室设备的准确性和稳定性,能进行熟练稳定操作的医护人员人数等因素,应用受限。实际上,面对疫情的爆发,需要多样、快速、灵敏、简便、成本较低的检验方法,来解决单一核酸检测的新方法假阴性及应用受限的难题。
相比于核酸诊断来看,免疫诊断是基于抗原、抗体间的特异性免疫反应来检测各种疾病的方法,根据其标记信号的不同,衍生出了各种不同的免疫诊断方法。从对实验室的要求来说,抗体检测对临床实验室的操作要求相对于核酸检验测试要低,可以快速、大量检测,且可以在基层实验室完成。
免疫诊断和核酸诊断的最大区别在于,核酸检测是为了检测COVID-19的特异性核酸,技术原理是先将新型冠状病毒RNA逆转为DNA,再将标本中的特定核酸序列进行扩增后检测。
免疫检测是通过抗体抗原之间的特异性反应原理,通过检测体内病毒蛋白(抗原)、或者体内特异性针对病毒蛋白的抗体,广泛应用于艾滋病病毒、乙型肝炎、丙型肝炎等重大传染病的检测。
病毒蛋白的检测一般有两种方式:一种是用抗体测抗原,这是找直接证据,测出抗原肯定是有感染了;另一种是用抗原(一般是重组的)测抗体,这是间接证据,人有了这个抗体,又不是通过打疫苗获得的,就间接证明感染了这个病原体。抗体是机体感染病毒后,体液免疫应答的产物。
但值得一提的是,检测和核酸检测两者并不冲突,也不能互相替代,都是病毒感染诊断的重要手段。
特异抗体检测阳性不能像病毒核酸检测阳性一样作为病毒感染的“金标准”。早期的病人抗体浓度低,甚至还没有产生免疫应答,受限于检测窗口期。同时,因为抗体检测容易受到血液标本中的一些干扰物质(如类风湿因子、非特异IgM、溶血所致的高浓度血红蛋白等)的存在而出现“假阳性”结果,所以抗体检测必须采用IgM和IgG同时检测且通常需多次动态检测来确认。
基于病毒蛋白的免疫学检测方案开发难点在于抗体原料的生产。与核酸检测试剂盒相比,免疫学检测试剂盒所需的开发时间更长,生产成本更高。
从适用场景来说,抗体检测检测速度快,操作简单,对于疑似病人快速检测排查具有重要意义。更适用于基层医疗机构、社区和乡镇卫生院的发热人群的筛查,对有效控制COVID-19的大规模传播具有重要的意义。
和核酸诊断相比,免疫诊断试剂盒还可以快速筛查无症状病毒携带者,可以用于机场、车站、码头等大流量公共场所的分布式筛查,为疫情的全面防控提和摸底调查提供技术支持。
据动脉网统计,目前已经有超过20家企业投入到新型冠状病毒(COVID-19)免疫诊断试剂研发中。
2月22日,国家药品监督管理局应急审批通过3家企业3个新型冠状病毒检测产品,其中包括2个胶体金法抗体检测试剂、1个恒温扩增芯片法核酸检测试剂,扩大了新型冠状病毒的检测的新方法和手段,全力服务疫情防控需要。这也是首次免疫学诊断试剂获批上市投入抗疫一线中。
接下来,3月1日,国家药品监督管理局对外发布通告,应急审批通过3家企业4个新型冠状病毒检测产品,包括2个化学发光法抗体检测试剂、2个荧光PCR法核酸检验测试试剂。
在3月1日的应急审批中,博奥赛斯(重庆)生物有限公司的新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(磁微粒化学发光法)和新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法)产品获批。
3月6日,国家药品监督管理局应急审批通过厦门万泰凯瑞生物技术有限公司1个新型冠状病毒(2019-nCoV)抗体检测试剂盒(化学发光微粒子免疫检测法)。
截至目前,共批准新冠病毒核酸检测试剂厂家10家,抗体检测试剂4家。抗体试剂获批厂家包括万孚生物、英诺特、博奥赛斯(重庆)生物有限公司、泰凯瑞生物。
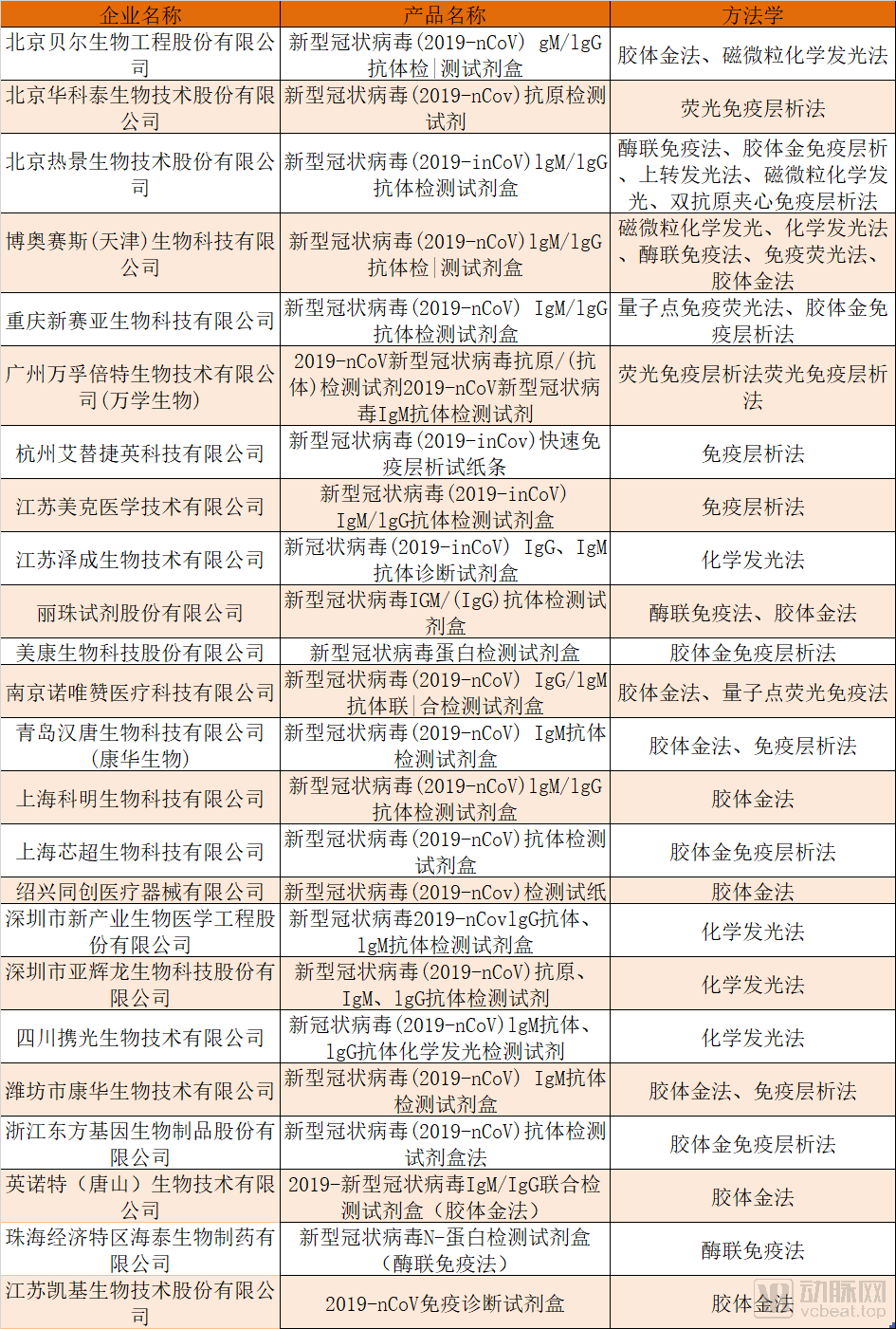
免疫诊断方法主要包括:放射免疫分析技术、免疫胶体金技术、酶联免疫分析技术、时间分辨荧光免疫分析技术和化学发光免疫分析技术,动脉网根据不同的方法学对已研发出产品的企业进行了整理。
2020年1月30日,热景生物针对新型冠状病毒免疫快速试剂和酶免试剂先后研发成功。
为应对新型冠状病毒肺炎疫情,热景生物“实验室”2020年1月15日启动研发,20日完成核酸试剂研发,21日开始基因重组蛋白表达,22日开始免疫试剂研发,30日免疫快速试剂和酶免试剂先后研发成功,现在已经研发了三款针对此次病毒的检测试剂盒。目前市面上用于新型冠状病毒感染的诊断方法均为病毒核酸检测,需要在专业的PCR实验室进行检测,平均检测时间为120分钟。因此疫情防控急需快速、简易筛查新型冠状病毒感染患者的诊断试剂盒。
热景生物成功克隆了新型冠状病毒外膜蛋白。并以病毒的该蛋白用做免疫诊断的抗原,研发出了15分钟快速出诊断结果的胶体金免疫检测试剂和上转发光免疫检测试剂。
丽珠集团2月13日晚公告,丽珠试剂与中国科学院武汉病毒研究所研制的新型冠状病毒IgM抗体检测试剂(胶体金法)、新型冠状病毒IgG抗体检测试剂(胶体金法)已通过体外诊断试剂应急审批答辩,并于2月11日进入快速审批通道。
同时由药品检定研究院、中国科学院武汉病毒研究所和丽珠试剂共同申报的科技部应急项目,新型冠状病毒IgM抗体检测试剂盒(酶联免疫法)也于2月11日进入国家应急审批通道。
美康生物研发的新型冠状病毒蛋白快速检测试剂盒,采用免疫层析法,是一种POCT快速检测方式。此方法通过分别标记在纳米颗粒上和固定在硝酸纤维膜检测区带上的特异性抗体,与样本中的新型冠状病毒蛋白抗原形成双抗体夹心的免疫反应,并运用纳米颗粒的显色作用,从而实现对特异性的新型冠状病毒蛋白的定性检测。该产品主要用于医疗机构对新型冠状病毒的初步快速筛查,最快10分钟可出结果。
南京诺唯赞医疗 新型冠状病毒(2019-nCoV) IgG/lgM抗体联合检测试剂盒
诺唯赞凭借量子点荧光免疫和胶体金产品开发的丰富经验,成功研发出新型冠状病毒(2019-nCoV)IgG/IgM抗体联合检测试剂盒(胶体金法)和新型冠状病毒(2019-nCoV)IgG/IgM抗体联合检测试剂盒(量子点荧光免疫法),新冠病毒IgM与IgG抗体联检试剂卡,现已通过江苏省医疗器械注册检验,并正在开展试剂盒的临床验证工作。
诺唯赞新冠病毒IgG/IgM抗体联合检测试剂盒能够全血10分钟初筛阳性患者,量子点荧光免疫法联检试剂盒能够帮助医院、疾控批量患者筛查和诊断;胶体金法联检试剂盒则适用于针对众多基层医院以及近期企业复工、学生返校的人群进行感染筛查。
1月29日,芯超生物新型冠状病毒(2019-nCoV)抗体检测试剂盒(胶体金免疫层析法)研制成功。
芯超生物研制成功的POCT快速检测试剂盒,运用免疫胶体金层析技术,实现对人体血清、血浆或全血中新型冠状病毒IgM/IgG抗体的体外定性检测,加样后15分钟内就可以观察结果。可以方便快速地用于该病毒感染患者在社区卫生服务中心、基层医院的早筛早诊,不但增加检测和诊疗的时效性,而且可以有效防止广大群众在大型医院密集检查而导致的交叉感染。
新型冠状病毒感染的肺炎疫情爆发后,同创医疗与感染性疾病诊治协同创新中心进行了紧密的科研技术攻关和转化合作,运用前期积累的技术储备,研制出了适合于现场筛查的新型冠状病毒检测试纸,只要将患者咽喉里的口水唾沫或者是鼻腔里的黏膜液采集到抽提管,再用该试纸进行检测,只需10分钟,便可根据检测线和对照线两条杠的显示,得出阳性或阴性结果。
2020年1月31日,潍坊市康华生物技术有限公司研发的胶体金法和免疫层析法新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒,通过了国家食品药品监督管理局济南医疗器械质量监督检验中心检验,成为我国法定检验机构检定合格的首个新型冠状病毒IgM抗体快速检测产品。目前正在向国家药监局申请应急审批,待取得注册证后,就能投入市场销售。
在获得国家药品监督管理局的上市批件后,这种快速诊断试剂盒将被发往各地医院,用于社区卫生服务中心、基层医院、三级医院门急诊、发热门诊的疑似人群的早筛早诊。此次通过注册检验的两个产品操作简便,样本覆盖全血、血清、血浆,最快3分钟即可出结果。单人份检测,无需仪器设备,适合现场筛查。
东方基因已成功研制出新型冠状病毒核酸检测试剂盒(免提取荧光PCR法)和新型冠状病毒抗原检测试剂(胶体金法),并已用于临床试验和科研试用,其中核酸检测试剂盒的临床试验准确率高达97%以上;胶体金法产品操作简单,可以将检测时间缩短至10分钟。
2020年2月8日,凯基生物与南京大学联合攻关,加速研制新冠病毒免疫诊断试剂盒。该产品是利用高通量纳米抗体筛选技术结合胶体金法开发的新型2019-nCoV免疫诊断试剂盒。
凯基生物利用免疫学方法,开发了半乳糖凝集素-3检测试剂盒、可溶性生长刺激表达基因2蛋白(ST2)检测试剂盒、D-二聚体检测试剂盒、肌钙蛋白I检测试剂盒等10几种检测试剂盒,在免疫技术领域积累了丰富的技术和经验。本试剂盒开发又利用了南京大学特有的高通量纳米抗体筛选技术,使得筛选的纳米单抗稳定性高(90℃条件下仍不会降解)、亲和力高、与人源抗体同源性超过 80%、毒性和免疫原性均较低,保证的试剂盒的稳定性、准确性。
华科泰拥有成熟的POCT技术平台,期望利用这一技术,可以为这场疫情攻坚战贡献自己的力量。春节期间,华科泰研发团队通过技术攻关,先后尝试了20种抗体配对,数百种技术方案,采用荧光微球免疫层析技术成功研发出2019-nCoV新冠病毒POCT快速免疫检测试剂盒。以咽拭子为检测样本,直接检测新冠病毒抗原,15分钟出结果,全力支援疫情检测。
万孚倍特 2019-nCoV新型冠状病毒抗原/(抗体)检测试剂2019-nCoV新型冠状病毒IgM抗体检测试剂
2020年1月20日,万孚生物旗下子公司万孚倍特公司宣布成功研发出新型冠状病毒呼吸道病原体多重核酸检测卡,检测组合根据国家卫生健康委办公厅印发的新型冠状病毒的肺炎诊疗方案(试行第二版)指导设置,包含新型冠状病毒及其他需要鉴别诊断的呼吸道病原体,结合万孚倍特独家专利的BoxArray(博科斯瑞)全自动多重核酸检测平台,打造出全自动全封闭的新型冠状病毒呼吸道病原体多重核酸检测模式。
美克医学第一时间召集技术团队组织新冠病毒肺炎检测技术攻关工作。团队以患者感染新冠病毒后体内产生的IgM/IgG抗体作为标的,研发出了15分钟内快速出结果的检测试剂盒。此系列免疫试剂结合其他临床指征,能够迅速、有效、定性进行医院临床诊断。
成都微康生物 新型冠状病毒(2019-nCoV)IgM、lgG抗体检测试剂盒
疫情发生后,成都微康生物联合四川大学华西医院,以微流控POCT诊断平台为基础,通过自主研发的新冠病毒特异性表位抗原和抗体,联合共聚焦时间分辨荧光免疫测试仪和微流控时间分辨荧光免疫技术开发出了该检测系统。使用血液作为样本、15分钟出结果,且检测灵敏度高达1pg/ml,CV仅为5%左右;采用特有的喷雾冷冻干燥技术,芯片可以常温保存,适合更多场景使用。
据悉,重庆医科大学联合博奥赛斯生物科技有限公司成功研发出新型冠状病毒(2019-nCoV)化学发光免疫检测试剂盒。该试剂盒具有检测快速、高通量和低成本的特点,可用于新冠肺炎的早期诊断、流行病学筛查和临床转归预测。该试剂盒的200例临床验证,由重医大附属永川医院、重庆三峡中心医院和市公共卫生医疗救治中心(均为重庆市指定的重症定点医疗救治医院)合作完成。
新型冠状病毒疫情发生以后,泽成生物快速启动新型冠状病毒2019-nCoV免疫检测试剂盒相关研究工作,在短时间内快速完成了2019-nCoV的IgG、IgM 血清学诊断试剂盒(化学发光法)的研发。
新产业生物 新型冠状病毒2019-nCovlgG抗体、lgM抗体检测试剂盒
新产业生物于2017年7月成为中国第一家获得美国FDA准入的化学发光厂家。2018年,新产业生物成功发布全球最快全自动化学发光免疫分析系统MAGLUMIX8。
新产业生物公司试剂研发出全自动化学发光新型冠状病毒2019-nCoV IgG抗体、新型冠状病毒2019-nCoV IgM抗体检测试剂盒。
新产业生物新型冠状病毒检测试剂盒最快可25分钟获得第一份检测结果,每小时可做300个测试,可全天候24小时全自动连续检测,使用血液样本,方便采集,助力筛查可疑病例。
亚辉龙生物 新型冠状病毒(2019-nCoV)抗原、IgM、lgG抗体检测试剂
亚辉龙第一时间就成立了抗原、抗体检测试剂攻坚小组。疫情突发至今,亚辉龙研发人员攻克了病毒特异性蛋白的基因工程表达、纯化和量产,并已完成新型冠状病毒(2019-nCoV)抗原、IgM抗体、IgG抗体检测的系列产品开发。
2020年2月4日,深圳天深医疗器械有限公司宣布,联合深圳市第三人民医院(国家感染性疾病临床研究中心)、深圳大学共同开展了2019新型冠状病毒IgM和IgG抗体检测试剂盒(化学发光法)研发成功。
目前该试剂盒正在深圳第三人民医院(国家感染性疾病临床研究中心)进行临床试验。初步临床实验显示发热7-14天病人临床样本IgM临床符合率96.6%(29/30),IgG临床符合率96.6%(29/30),同时公司也正在对更大的临床样本进行验证。相关试剂盒的注册报证进度正在进行中。
成都微康生物科技有限公司创始人、CEO 唐勇博士告诉动脉网:“针对新型冠状病毒快速免疫检测试剂研发的核心痛点是找到病毒特异性的抗原和高度特异性的表位抗体。目前大部分成品免疫检测试剂盒都以常规冠状病毒抗原为基础,缺少特异性,容易造成误诊和漏诊。 ”
除此以外,他也指出现在停滞的物流也将给免疫诊断产品下沉基层带来挑战,他表示:“目前大部分免疫检测试剂都需要冷链运输,在疫情爆发下,物流和冷链基本停滞,基层医院的冷链运输更无从谈起,无法保证试剂性能。但短时间内很多公司没办法改变试剂形态和储存方式。“
核算检验测试出现的漏诊问题,免疫诊断也有可能出现。因为目前的新冠病毒IgM或IgG胶体金检测试剂灵敏度低,出现假阴性,易造成漏诊。同时,由于大部分的胶体金检测是选择N蛋白作为检测靶点,但是N蛋白跟其他冠状病毒的同源性较高,特异性低易造成假阳性,导致漏诊。
天深医疗董事长姚天成告诉动脉网:”正常的审批需要3年,应急审批需要1-2月。而审批中的影响因素需要考虑企业在应急审批之后,其产品能否快速、大规模、有效应用于疫情防控,具体条件,需要参考国家食药监局的的要求。“
在2020年2月12日,国家药品监督管理局医疗器械技术审评中心发布了《2019新冠病毒核酸检测试剂注册技术审评要点》,但目前还未发布关于抗原/抗体检测试剂审评要点相关信息。
在2003年的非典疫情中,军事医学科学院、中科院北京基因组所、华大基因等单位都开发出了可以检测SARS病毒本身,或患者对病毒免疫反应的ELISA试剂盒。而在这次疫情中,也有多家企业的产品已经进入审批通道,我们希望随着一批免疫检验测试产品的上市,帮助防疫控疫单位快速筛查感染者和潜在感染者,摸清疫情流行情况。